De las ancas de rana a las baterías: ¿Cómo funciona un almacenamiento de energía?
Un poco de historia: El descubrimiento de la electricidad
Luigi Galvani era un médico italiano y científico curioso del siglo XVIII. Durante un experimento para investigar músculos de ancas de rana, descubrió una conexión entre metales apilados y la contracción de las ancas de rana. Cuando Galvani tocó accidentalmente los músculos con una barra de latón contra una rejilla metálica, estos se contrajeron. Tenía claro que la electricidad había jugado un papel aquí – pero qué había sucedido exactamente solo se determinó algunos años después.
El físico italiano Alessandro Volta reconoció, basándose en el descubrimiento de Galvani, que con la ayuda de dos discos de metal diferentes y un disco de cuero empapado en agua salada entre ellos se puede generar voltaje eléctrico. Volta apiló primero un disco de zinc, luego un disco de cuero húmedo y finalmente un disco de plata. Repitió esto varias veces y creó la pila voltaica – la primera batería técnicamente aplicable.
En honor a estos descubrimientos científicos:
- La unidad física de voltaje (Voltio) recibió el nombre de Volta
- La combinación de discos de zinc, plata y cuero se denominó celda galvánica
La celda galvánica constituye la base de todas las celdas de batería modernas.
Algunos fundamentos: Metales nobles y no nobles
¿Qué tiene de especial la combinación de plata, zinc y cuero empapado en sal? Para responder a esto, primero deben explicarse algunos términos básicos.
La capacidad de ceder y aceptar electrones de los metales es el elemento fundamental para describir el funcionamiento de una batería:
| Tipo de metal | Propiedades | Ejemplos |
|---|---|---|
| Metales nobles | No se oxidan, reaccionan poco con otras sustancias, retienen electrones y pueden absorber más | Plata, Oro, Platino |
| Metales no nobles | Muy reactivos, se oxidan, ceden electrones | Zinc, Hierro, Aluminio |
Los términos más importantes de la tecnología de baterías
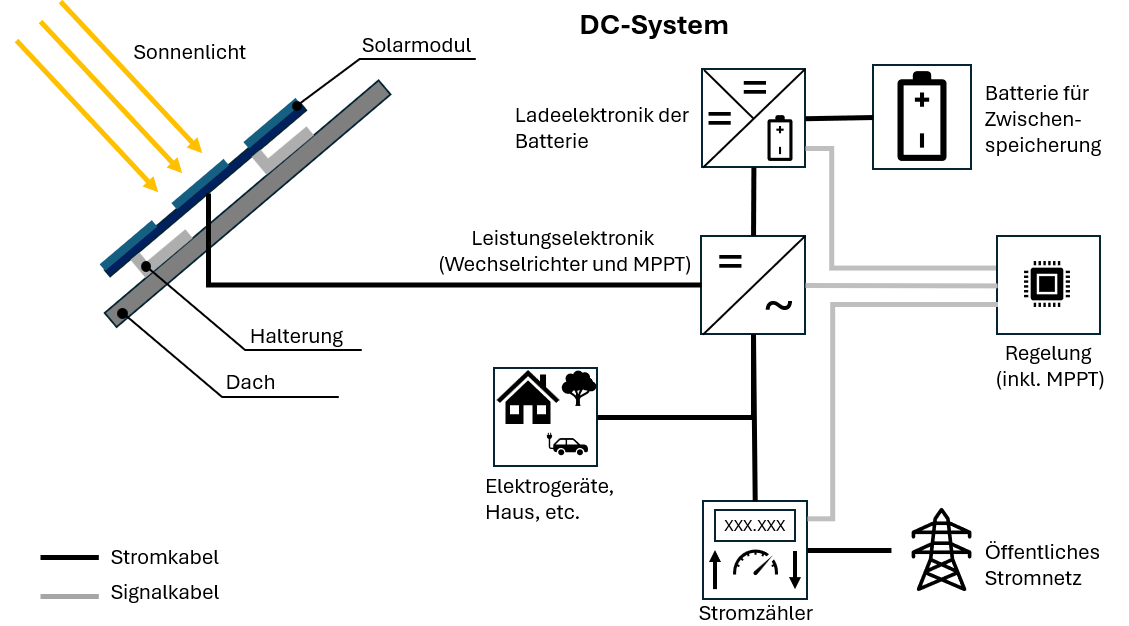
Ánodo: El electrodo negativo (polo negativo), consiste en material no noble, cede electrones.
Cátodo: El electrodo positivo (polo positivo), consiste en material noble, absorbe electrones.
Electrolito: Un líquido o sólido que puede conducir corriente eléctrica mediante partículas cargadas (iones).
Separador: Separa ánodo y cátodo, pero deja pasar iones – evita cortocircuitos.
Principio de funcionamiento en detalle: El proceso de descarga
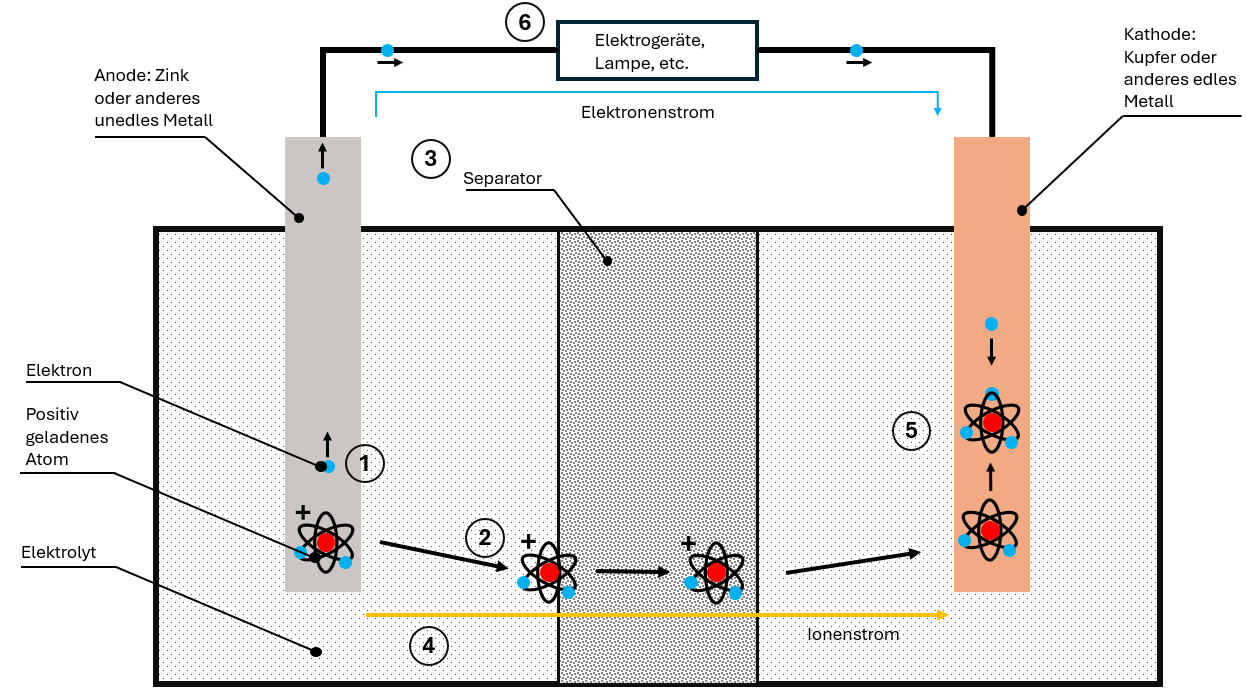
La celda de batería estándar se compone de cuatro componentes:
- Ánodo (polo negativo)
- Cátodo (polo positivo)
- Electrolito
- Separador
Así funciona la descarga:
- Cesión de electrones: El ánodo no noble cede electrones que migran por el cable hacia el cátodo
- Formación de iones: Por la falta de electrones se forman iones cargados positivamente en el ánodo
- Migración de iones: Los iones se disuelven en el electrolito y migran a través del separador hacia el cátodo
- Dos corrientes separadas:
- Corriente de electrones por el cable (¡utilizable!)
- Corriente de iones por el electrolito
- Reunificación: En el cátodo, electrones e iones se reúnen de nuevo
La corriente de electrones es corriente continua – fluye siempre en una dirección y puede utilizarse para dispositivos eléctricos. La energía química se convierte así en energía eléctrica.
El proceso de carga: Todo al revés
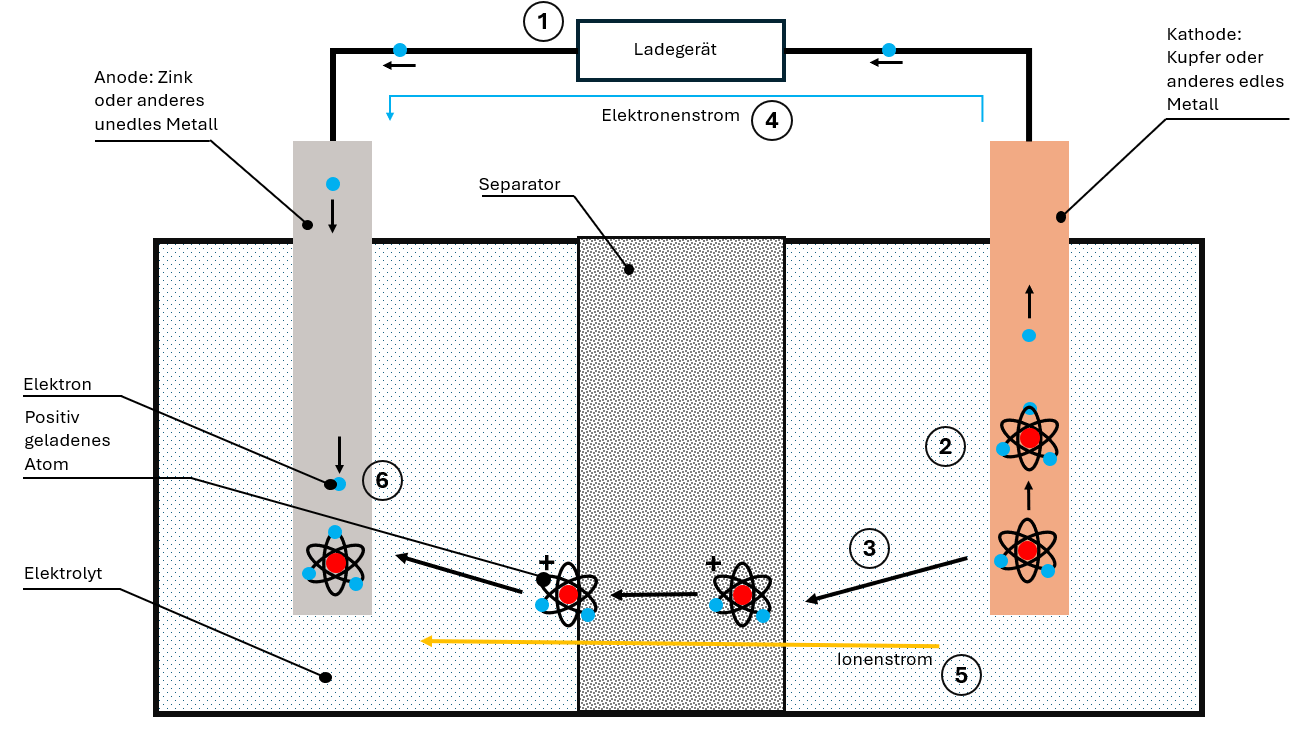
Al cargar, el cargador aplica un voltaje opuesto. Con ello, todo el proceso se invierte:
- El cátodo "pierde" sus electrones, que migran hacia el ánodo
- Los iones se desprenden del material del cátodo
- Los iones se mueven a través del electrolito y el separador hacia el ánodo
- En el ánodo, iones y electrones se almacenan de nuevo
La batería está recargada y lista para el siguiente ciclo de descarga.
Términos técnicos y unidades importantes
Vida útil y ciclos de carga
Un ciclo de carga es el proceso de una descarga y carga completa. Las baterías modernas de iones de litio alcanzan, según el tipo, entre 1.000 y 4.000 ciclos.
Profundidad de descarga (DoD – Depth of Discharge)
La profundidad de descarga indica en qué porcentaje se ha descargado la batería:
- 0% DoD = Batería completamente cargada
- 100% DoD = Batería completamente descargada (¡evitar!)
Cada tipo de batería tiene una profundidad de descarga máxima recomendada. Si se sobrepasa, la batería se daña.
Tasa C: Velocidad de carga y descarga
La tasa C describe la relación entre potencia de carga/descarga y capacidad:
Tasa C = Potencia (kW) / Capacidad (kWh)
| Tasa C | Tiempo de carga/descarga | Significado |
|---|---|---|
| 0,25C | 4 horas | Carga suave |
| 0,5C | 2 horas | Estándar almacenamiento doméstico |
| 1C | 1 hora | Carga rápida |
| 2C | 30 minutos | Alto rendimiento |
Ejemplo: Una batería con 10 kW de potencia y 20 kWh de capacidad tiene una tasa C de 0,5C – se carga o descarga en 2 horas.
Densidad energética
La relación entre energía almacenada y espacio ocupado:
- Volumétrica: Wh por litro (Wh/l)
- Gravimétrica: Wh por kilogramo (Wh/kg)
Las baterías de iones de litio con cátodos LFP alcanzan aproximadamente 200 Wh/kg – significativamente más que las baterías de plomo-ácido.
Efecto memoria
Este fenómeno describe la reducción de capacidad al cargar una batería no completamente descargada. La batería "recuerda" el ciclo de carga acortado y solo entrega una parte correspondiente de la capacidad.
Importante saber: Las baterías modernas de iones de litio prácticamente no se ven afectadas por el efecto memoria – a diferencia de las antiguas baterías de níquel-cadmio.
Resumen: Las unidades más importantes
Para trabajar con baterías y sistemas solares, algunas unidades e indicadores son especialmente importantes. La siguiente tabla resume las magnitudes esenciales:
| Unidad | Nombre | Significado |
|---|---|---|
| kW | Kilovatio | Potencia (trabajo por tiempo) |
| kWh | Kilovatio-hora | Cantidad de energía (1 kW durante 1 hora) |
| kWp | Kilovatio pico | Potencia máxima del sistema solar |
| % (η) | Eficiencia | Energía aprovechable / energía empleada |
| C | Tasa C | Potencia de carga/descarga / Capacidad |
| % DoD | Depth of Discharge | Profundidad de descarga |
Conclusión
Resumen: El principio de funcionamiento de la batería se basa en la celda galvánica y reacciones químicas. Con un ánodo, cátodo, separador y electrolito se separan electrones e iones – así surge voltaje eléctrico utilizable. Lo que comenzó hace más de 200 años con ancas de rana y discos de metal es hoy la base de teléfonos inteligentes, coches eléctricos y sistemas solares.
Continúa en: En el siguiente artículo Litio vs. Plomo: ¿Qué batería para el sistema solar? comparamos las dos tecnologías de batería más importantes para el uso en sistemas solares.
La serie completa "Almacenamiento de energía para sistemas solares"
- De las ancas de rana a las baterías: ¿Cómo funciona un almacenamiento de energía? – Está aquí
- Litio vs. Plomo: ¿Qué batería para el sistema solar? – Comparación de tecnologías
- Electrónica de potencia: Inversores y convertidores DC-DC – Conversión de corriente
- El todoterreno: Inversor híbrido – Todo en un dispositivo
- ¿AC o DC? Topologías de sistemas para instalaciones solares – Conceptos de instalación
